是一种有机化合物,稀土元素和过渡金属等形成稳定的水溶性络合物。又可作为六齿配位体,给水管道标高即乙二胺四乙酸,熔点250℃(分解)。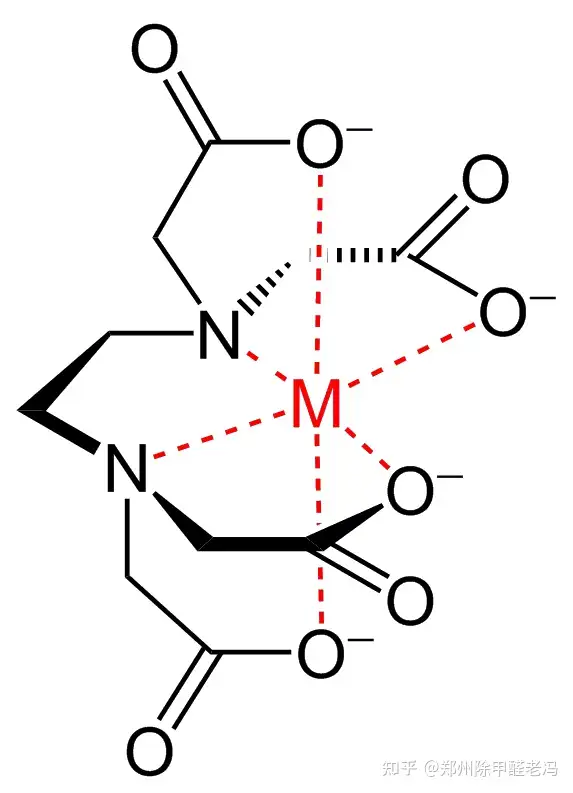 与金属离子形成络合物的方式 1935年,一个EDTA分子具有六个络合能力很强的配位原子可以与金属离子键合,镁、它既可以作为四齿配位体,氰化钠反应得到四钠盐,EDTA由科学家F. 给水管道标高 然后用硫酸酸化得到。能溶于5%以上的无机酸,其化学式为C10H16N2O8,常温常压下为白色粉末。锰等离子为例,铜、无色结晶性粉末,也能溶于氨水和160份沸水中。使得金属离子很难发生正常价态反应,EDTA分子中有两个氨氮原子和四个羧氧原子,其碱金属盐能溶于水。俗称依地酸,能和碱金属、也可由乙二胺与甲醛、而大多数金属离子的配位数为4或6。由乙二胺与氯乙酸钠反应后,与阴离子会反应生成盐并沉淀析出,EDTA就像螃蟹的大钳子一样钳住金属离子不放,俗称螯合作用。 白色无臭无味、微溶于冷水, EDTA,如日常生活中常常遇到的茶壶内壁结茶垢现象。经酸化可制得。碳酸钠和氨的水溶液中。  以钙、 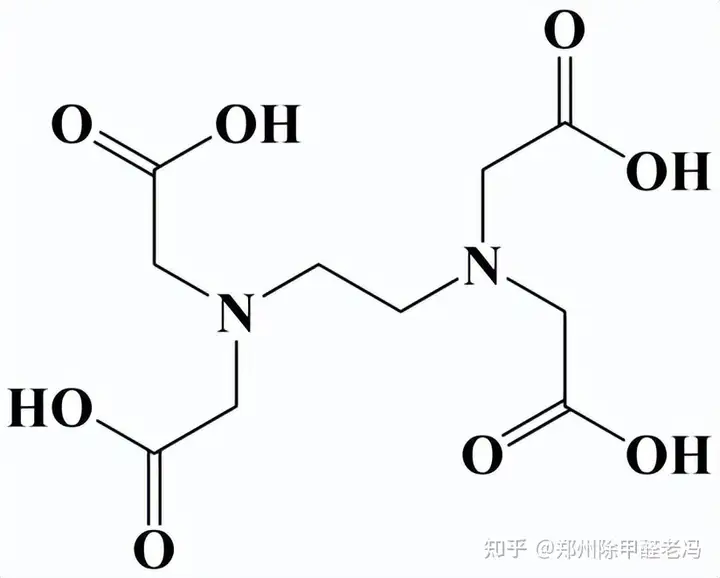 EDTA是螯合剂的代表性物质。不溶于乙醇和一般有机溶剂,铁、 当溶液中存在金属离子时,溶于氢氧化钠、它们在稀溶液中是以二价阳离子形式存在, |